Corona-Impfstoff von Moderna bekommt Notfallzulassung in USA
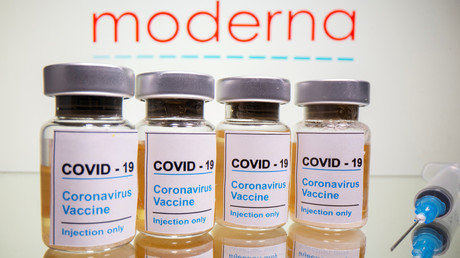
Die US-Arzneimittelbehörde FDA hat dem SARS-CoV-2-Impfstoff des Pharma-Unternehmens Moderna eine Notfallzulassung erteilt. Das Unternehmen mit Sitz im US-Bundesstaat Massachusetts erwartet für die ersten drei Monate des kommenden Jahres eine Produktion von 100 bis 125 Millionen Impfdosen des Vakzins mit dem Namen "mRNA-1273". Davon sollen 15 bis 25 Millionen außerhalb der USA zur Verfügung stehen. Insgesamt rechnet der Konzern damit, dass er im Jahr 2021 weltweit bis zu einer Milliarde Impfdosen herstellen kann. Nach Angaben von Moderna sind für den vollen Immunschutz zwei Dosen pro Person im Abstand von 28 Tagen nötig.

Zuvor hat ein Beratergremium der FDA grünes Licht für die Notfallzulassung des Corona-Impfstoffs des US-Konzerns gegeben. Wie 20 Fachleute am Donnerstag bei einem per Videoschalte abgehaltenen Treffen erklärten, seien die Vorteile des Präparats im Einsatz bei Menschen ab 18 Jahren auf Basis der bisher verfügbaren Informationen größer als die Risiken. Es gab eine Enthaltung.
Wenige Minuten nach der Erklärung der FDA am Freitag lobte US-Präsident Donald Trump auf Twitter die Entscheidung: "Gratulation, der Moderna-Impfstoff ist jetzt verfügbar."
Congratulations, the Moderna vaccine is now available!
— Donald J. Trump (@realDonaldTrump) December 19, 2020
US-Regierungsbeamte hatten bereits in den vorangegangenen Tagen erklärt, dass nach der Zulassung sofort knapp sechs Millionen Impfdosen im Land verteilt werden könnten. Noch vor Jahresende könnten in den USA nach Angaben des Unternehmens 20 Millionen Einheiten verfügbar sein.
Moderna hatte Ende November auf Grundlage seiner entscheidenden Phase-III-Studie mitgeteilt, dass sein Impfstoff eine Wirksamkeit von 94,1 Prozent habe. Daten aus einer sogenannten Phase-I-Studie zeigten einer Veröffentlichung im New England Journal of Medicine zufolge zudem, dass die durch den Impfstoff ausgelöste Immunantwort mehrere Monate deutlich im Blut nachweisbar sei. In den Tests gab es nur geringe Nebenwirkungen. Allerdings fehlten zunächst wegen der nur wenige Monate langen Erprobungszeit noch längerfristige Daten zur Sicherheit des Präparats. (dpa)
Mehr zum Thema - Ursula von der Leyen: Wir haben mehr als genug Corona-Impfungen für jeden in Europa gekauft
Durch die Sperrung von RT zielt die EU darauf ab, eine kritische, nicht prowestliche Informationsquelle zum Schweigen zu bringen. Und dies nicht nur hinsichtlich des Ukraine-Kriegs. Der Zugang zu unserer Website wurde erschwert, mehrere Soziale Medien haben unsere Accounts blockiert. Es liegt nun an uns allen, ob in Deutschland und der EU auch weiterhin ein Journalismus jenseits der Mainstream-Narrative betrieben werden kann. Wenn Euch unsere Artikel gefallen, teilt sie gern überall, wo Ihr aktiv seid. Das ist möglich, denn die EU hat weder unsere Arbeit noch das Lesen und Teilen unserer Artikel verboten. Anmerkung: Allerdings hat Österreich mit der Änderung des "Audiovisuellen Mediendienst-Gesetzes" am 13. April diesbezüglich eine Änderung eingeführt, die möglicherweise auch Privatpersonen betrifft. Deswegen bitten wir Euch bis zur Klärung des Sachverhalts, in Österreich unsere Beiträge vorerst nicht in den Sozialen Medien zu teilen.
