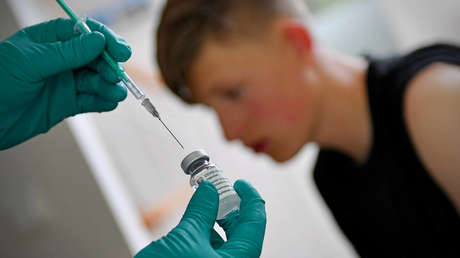
Studie auch in Deutschland: Pfizer/BioNTech wollen Corona-Impfstoff ab 3. Lebensjahr testen
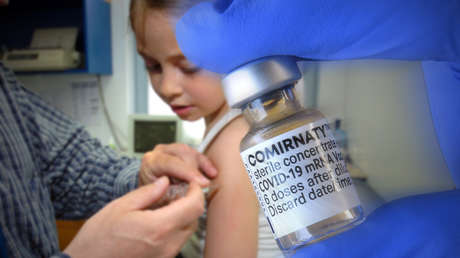
Ende Mai war es soweit: Wie viele Beobachter erwartet hatten, gab die Arzneimittelagentur EMA der Europäischen Union grünes Licht für die Impfungen mit Vakzinen der Pharmaunternehmen BioNTech/Pfizer für Kinder und Jugendliche ab dem Alter von 12 Jahren. Auch für Bundesgesundheitsminister Jens Spahn war das "eine großartige Nachricht". Umgehend erteilte auch die EU-Kommission offiziell die entsprechende Zulassung für alle 27 Mitgliedsländer.

Von der Ständigen Impfkommission (STIKO) in Deutschland gab es jedoch noch keine Empfehlung bislang. Laut Stimmen aus dem Deutschen Bundestag solle erst eine solche Empfehlung die notwendige "Voraussetzung für eine eventuelle Corona-Impfung von Kindern" in Deutschland sein.
Währenddessen planen der US-Branchenprimus Pfizer und der deutsche Impfstoff-Durchstarter BioNTech bereits den nächsten Schritt. Die Altersgrenze zur Verabreichung des hauseigenen Corona-Impfstoffs soll noch weiter abgesenkt werden – auf Kleinkinder ab zwei Jahren.
"Diese Studie wird in den Vereinigten Staaten, Brasilien und Deutschland durchgeführt."
Wie aus den Informationen zur klinischen Studie NCT 04895982 mit Stand 21. Mai hervorgeht, strebe man danach festzustellen, ob der eigene mRNA-Impfstoff BNT162b2 auch schon für die ganz jungen Erdenbürger "sicher und verträglich" ist.
Es handelt sich um eine sogenannte Dreifach-Impfstudie mit insgesamt 360 "immungeschwächten" Teilnehmern ab einem Lebensalter von zwei Jahren (180 Erwachsene, 180 Kinder).
"Männliche oder weibliche Teilnehmer, die zum Zeitpunkt der Teilnahme mindestens 2 Jahre alt sind."
Die Probanden sollen laut Studienkonzeption über einen Zeitraum von sechs Monaten nach Verabreichung der dritten Impfdosis unter Beobachtung stehen. Die Studie selbst, so heißt es, werde sich über einen Zeitraum von 14 Monaten erstrecken.
Vorerkrankungen sind demnach eine notwendige Vorbedingung für die Teilnahme an der Impf-Studie. Zu solchen zählen zum Teil erhebliche Einschränkungen der Gesundheit u.a. durch eine Chemotherapie oder eine Organ-, Knochenmark- bzw. Stammzellentransplantation. Die Lebenserwartung der potentiellen Teilnehmer muss jedoch noch bei mindestens 12 Monaten liegen ("Life expectancy ≥12 months").
Was die teilnehmenden Kinder und Jugendlichen anbelangt, sollten "alle Eltern/Erziehungsberechtigten (…) vollständig informiert werden, und die Teilnehmer sollten so weit wie möglich über die Studie in einer Sprache und in Begriffen, die sie verstehen können, informiert werden".
Von der Teilnahme ausgeschlossen werden – wie aus den zur Verfügung gestellten Informationen hervorgeht – solche Menschen, die bereits eine schwere Impf-Reaktion aufwiesen und/oder eine schwere allergischen Reaktion (z. B. Anaphylaxie) entwickelten.
Die Bewertung der vorgesehenen Intervention werde (mit Stand 17. Mai) anhand der folgenden Ergebnisparameter vorgenommen:
- Prozentsatz der Teilnehmer, die über lokale Reaktionen berichten (Zeitrahmen: Für 7 Tage nach Dosis 1, Dosis 2 und Dosis 3), Schmerzen an der Injektionsstelle, Rötung und Schwellung
- Prozentsatz der Teilnehmer, die über sogenannte systemische Ereignisse berichten (Zeitrahmen: Für 7 Tage nach Dosis 1, Dosis 2 und Dosis 3). Unter diesen befinden sich: Fieber, Müdigkeit, Kopfschmerzen, Schüttelfrost, Erbrechen, Durchfall, neu aufgetretene oder verschlimmerte Muskelschmerzen, neu aufgetretene oder verschlimmerte Gelenkschmerzen
- Prozentsatz der Teilnehmer, die über (auch erhebliche) unerwünschte Reaktionen berichten (Zeitrahmen: Von Dosis 1 bis 1 Monat nach Dosis 2)
- GMT-Wert (geometrischer mittlerer Titer) aller Teilnehmer, gemessen durch SARS-CoV-2-neutralisierende Titer, ohne serologischen oder virologischen Nachweis einer früheren SARS-CoV-2-Infektion und mit einem immungeschwächten Zustand, wie im Protokoll angegeben (Zeitrahmen: 1 Monat nach Dosis 2).
Die Rekrutierung potenzieller Probanden habe laut Studieninformationen bisher noch nicht begonnen. Die Studie soll am 1. September 2021 beginnen und am 4. Januar 2023 abgeschlossen sein.
Mehr zum Thema - Neue Studie bestätigt: Kein Grund für eiliges Impfen von Kindern
Durch die Sperrung von RT zielt die EU darauf ab, eine kritische, nicht prowestliche Informationsquelle zum Schweigen zu bringen. Und dies nicht nur hinsichtlich des Ukraine-Kriegs. Der Zugang zu unserer Website wurde erschwert, mehrere Soziale Medien haben unsere Accounts blockiert. Es liegt nun an uns allen, ob in Deutschland und der EU auch weiterhin ein Journalismus jenseits der Mainstream-Narrative betrieben werden kann. Wenn Euch unsere Artikel gefallen, teilt sie gern überall, wo Ihr aktiv seid. Das ist möglich, denn die EU hat weder unsere Arbeit noch das Lesen und Teilen unserer Artikel verboten. Anmerkung: Allerdings hat Österreich mit der Änderung des "Audiovisuellen Mediendienst-Gesetzes" am 13. April diesbezüglich eine Änderung eingeführt, die möglicherweise auch Privatpersonen betrifft. Deswegen bitten wir Euch bis zur Klärung des Sachverhalts, in Österreich unsere Beiträge vorerst nicht in den Sozialen Medien zu teilen.
