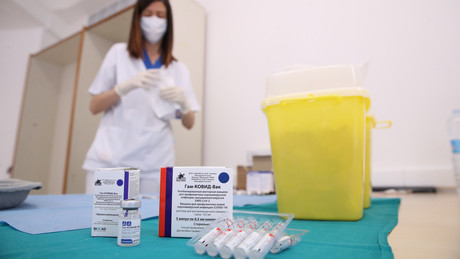
Europäische Arzneimittel-Agentur bewertet klinische Sputnik-V-Studien positiv
Experten der Europäischen Arzneimittel-Agentur (EMA) haben das Verfahren der klinischen Prüfung des Impfstoffs gegen das Coronavirus Sputnik V positiv bewertet. Dies gab Denis Logunow, stellvertretender Direktor des Gamaleja-Zentrums, das das Medikament entwickelt hat, am Dienstag bekannt. Auf dem Youtube-Kanal "SolovievLive" sagte er:
"Dies ist der Teil der Arbeit, bei dem es um die Anerkennung von Produktionsstandards geht, um die Anerkennung der Art und Weise, wie klinische Prüfungen durchgeführt wurden, dies ist der Teil, zu dem die EMA bereits gekommen ist und zu dem wir keine kritischen Anmerkungen haben. Zur Durchführung klinischer Prüfungen haben wir eine positive Stellungnahme erhalten."
Laut Logunow ist das Gamaleja-Zentrum nun dabei, die Standards für die Impfstoffproduktion mit der EMA zu harmonisieren. Er wies darauf hin, dass die Produktionsstandards in Europa, China und Russland miteinander harmonisiert werden müssen. Logunow fügte hinzu:
"Es ist ein solcher Prozess, und ich hoffe wirklich, dass wir ihn in absehbarer Zeit, in ein paar Monaten, abschließen können."
Im Oktober 2020 hatte der Russische Direktinvestitionsfonds (RDIF) bei der Weltgesundheitsorganisation (WHO) die beschleunigte Registrierung und Requalifizierung von Sputnik V beantragt. Im Januar hatte der Fonds die Zulassung von Sputnik V bei der EMA beantragt.

Im Juli letzten Jahres zitierte die Nachrichtenagentur Reuters Quellen, die über die Gründe für die Verzögerung des EMA-Zulassungsverfahrens für Sputnik V schrieben. Der Agentur zufolge hatte der Projektträger nicht die erforderlichen Daten über die Übereinstimmung der Master Cell Bank mit einer der EU-Verordnungen vorgelegt. Die Inspektoren hatten Fragen zur Berichterstattung über unerwünschte Wirkungen nach der Impfung während der Versuche – es war nicht klar, wie die Wissenschaftler die Ergebnisse bei denjenigen überwacht hatten, die ein Placebo erhalten hatten. Unzureichende Daten hätten das Genehmigungsverfahren für Sputnik V ins Stocken gebracht, berichtete die Agentur.
Der RDIF antwortete, der Artikel enthalte grobe Fehler und falsche Fakten. Der Fonds ist auch der Ansicht, dass das russische Medikament unter dem Druck der internationalen Pharmalobby steht. Im Oktober hatte Reuters unter Berufung auf vertrauenswürdige Quellen geschrieben, dass die EMA die Verwendung von Sputnik V im ersten Quartal dieses Jahres genehmigen könnte.
Mehr zum Thema - Gamaleja-Zentrum rät nach Pfizer-Empfehlung von COVID-19-Auffrischungsimpfung alle drei Monate ab
Durch die Sperrung von RT zielt die EU darauf ab, eine kritische, nicht prowestliche Informationsquelle zum Schweigen zu bringen. Und dies nicht nur hinsichtlich des Ukraine-Kriegs. Der Zugang zu unserer Website wurde erschwert, mehrere Soziale Medien haben unsere Accounts blockiert. Es liegt nun an uns allen, ob in Deutschland und der EU auch weiterhin ein Journalismus jenseits der Mainstream-Narrative betrieben werden kann. Wenn Euch unsere Artikel gefallen, teilt sie gern überall, wo Ihr aktiv seid. Das ist möglich, denn die EU hat weder unsere Arbeit noch das Lesen und Teilen unserer Artikel verboten. Anmerkung: Allerdings hat Österreich mit der Änderung des "Audiovisuellen Mediendienst-Gesetzes" am 13. April diesbezüglich eine Änderung eingeführt, die möglicherweise auch Privatpersonen betrifft. Deswegen bitten wir Euch bis zur Klärung des Sachverhalts, in Österreich unsere Beiträge vorerst nicht in den Sozialen Medien zu teilen.