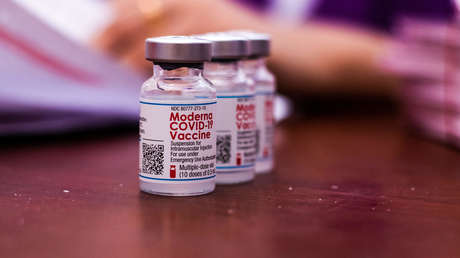
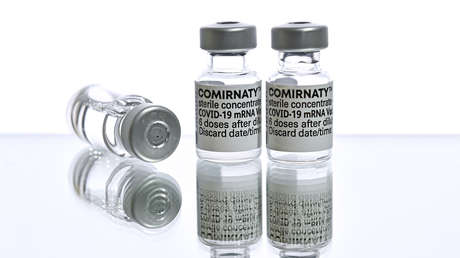
Verunreinigungen in den mRNA-Impfstoffen? Frühere EMA-Untersuchungen liefern Hinweise
von Maria Müller
Sucht man nach den Ursprüngen mancher sogenannter Verschwörungstheorien über die Gen-Impfstoffe, findet man viele Hinweise. Sie haben ganz offensichtlich ihre Wurzeln in den Themen der ersten umfassenden Prüfungs- und Zulassungsdokumente der Europäischen Arzneimittel-Agentur (EMA). Das zeigt sich am Beispiel des Vakzins Comirnaty. Die Texte spiegeln die Probleme einer neuen Technologie für Medikamente wider, die trotz zahlreicher Unsicherheiten, Schwächen und Improvisationen bereits im Anfangsstadium für die Menschheit freigegeben wurden. Nur die Pandemie ermöglichte den Sprung in die Zulassung, wenn auch unter Auflagen. Doch bis heute haben Pfizer/BioNTech bedeutende Forderungen der EMA nicht erfüllt, die als Hauptvoraussetzungen für die bedingte Zulassung gelten. (Assessment Report 19.02.2021 und aktualisierte Produktbeschreibung, 14.10.2021, S. 39)
Das am 21. Dezember veröffentlichte und am 19. Februar aktualisierte, doch wenig bekannte Grundlagendokument ist ein Gemeinschaftsprodukt des Ausschusses für Humanarzneimittel (CHMP), des Ausschusses für Risikobewertung im Bereich der Pharmakovigilanz (PRAC) und der Epidemie-Einsatzgruppe (ETF) der EMA. Es wurde nicht in andere europäische Sprachen übersetzt, wie bei Dokumenten der EU-Kommission sonst üblich. Das widerspricht der öffentlichen Transparenzverpflichtung. Ein großer Teil der europäischen Bevölkerung hat deshalb keinen Zugang dazu.

Der komplexe Arbeitsprozess der Kontrollausschüsse
Die Qualitätsprobleme des Impfstoffes stehen in dem 140 Seiten starken Text im Vordergrund. Themen wie die Produktinkonsistenz, die unterschiedlichen Chargenqualitäten oder mögliche Verunreinigungen samt unbekannter Gesundheitsfolgen wurden in einem hochkomplexen Arbeitsprozess diskutiert. Man definierte Prüf- und Kontrollverfahren und charakterisierte manche mögliche Gefahr als unterschwellig, zumal bei nur zwei autorisierten Dosen. Die EMA-Experten bezeichneten Erklärungen und gelieferte Daten der Pharmafirmen häufig als "akzeptabel", kritisierten jedoch auch immer wieder ungenügende Informationen und fehlende Studien. Vor allem die Vergleichbarkeit des klinischen Impfstoffes der Zulassungstestreihen mit dem kommerziellen Vakzin für Millionen Menschen wurde mehrfach eingefordert und war dann schließlich "akzeptabel".
Das alles erfinden nicht Querdenker oder "rechtsradikale Verschwörungstheoretiker", das bringt die Arbeit der wissenschaftlichen Experten der europäischen Zulassungsbehörde zutage. Erstaunlich, dass ihre Dokumente bis jetzt noch nicht gelöscht wurden. Man ist heutzutage dankbar für so viel Ehrlichkeit.
Ein schockierender Anlass, um den Text erneut zu lesen
Mein Rückgriff auf den Grundlagentext über mRNA-Stoffe hat einen aktuellen Anlass. Ende September zeigten Ärzte aus Deutschland und Österreich auf einer Pressekonferenz schockierende elektronenmikroskopische Aufnahmen von Verunreinigungen in verschiedenen mRNA-Impfstoffen. Man sah kleine, spitze Metallteilchen, langgezogene kettenartige Objekte, aber auch solche mit einer rechteckigen oder dreieckigen Form. Videos zeigten, wie sich winzige Teilchen dynamisch bewegten. Auf Blutbildern von geimpften Personen konnte man bisher unbekannte Teilchen verschiedener Form erkennen, die beobachtende Ärzte der Gruppe zugesandt hatten. Sie benutzten u. a. 600-fache Vergrößerungen.



An dieser Pressekonferenz nahm auch eine Medizinerin aus Österreich per Zoom teil, die ebenfalls mit einer Gruppe von Kollegen Reste von diversen Imfpstoffen auf Verunreinigungen ohne Unterbrechung der Kühlkette untersucht. Sie berichtete davon, dass sich mehrere Analyseteams gebildet hatten, die bereits seit Juni systematisch vorgehen. Sie arbeiten auch zum Thema der Impfstoffrechte. Die Ärztegruppe ist weltweit vernetzt.
"Es gibt 35 internationale Wissenschaftlergruppen, die gegenwärtig Impfstoffverunreinigungen prüfen. Wir haben Hunderte solcher Bilder, die wir mit dem Dunkelfeldmikroskop gesehen haben", sagte die Ärztin für Allgemeinmedizin.
Die Österreichische Ärztekammer drohte ihr bereits mit einem Disziplinarverfahren. Eine Gruppe von über 120 Ärztinnen und Ärzten bildet die Initiative "Wir zeigen unser Gesicht". Diese fühlt sich der Wahrheit verpflichtet.
Sichtbare Verunreinigungen in Impfstoffen
Auf der Pressekonferenz konnte man zum ersten Mal sehen, was man sich unter einer Verunreinigung von Gen-Impfstoffen vorzustellen hat. Die warnenden Sätze aus dem EMA-Dokument scheinen sich in diesen Bildern auszudrücken. Gleichwohl eröffnen sie Einblicke in Verunreinigungen, die selbst den EMA-Experten wohl nicht bekannt waren. Die Prüfungskommissionen der EMA müssten die Aufnahmen untersuchen. Auch das Paul-Ehrlich-Institut steht in der Verantwortung. Anstatt die Ärzte zu verunglimpfen, sollte man solche Befunde dankbar entgegennehmen und konstruktiv prüfen. Das wäre ein souveränes wissenschaftliches Vorgehen.
Schlaglichter auf Problembereiche
Zum besseren Verständnis seien einzelne Sätze aus dem Bewertungsbericht der EMA zitiert. Damit sollen und können nur einige Problembereiche hervorgehoben werden. Sie verdeutlichen, dass man Verunreinigungen verschiedenster Ursachen im Impfstoff Comirnaty festgestellt und untersucht hat.
Verunreinigungen durch das Lipidmaterial der Nanopartikel
Lipid ist das fettartige Umhüllungsmaterial der Nanopartikel, in dem die genetische Substanz eingebettet ist. Zitate:
"Lipidbezogene Verunreinigungen wurden in einigen kürzlich hergestellten Fertigproduktchargen beobachtet. Für die Chargen mit lipidbezogenen Verunreinigungen bleiben die bestehenden Qualitätskontrollparameter einschließlich der RNA-Integrität unverändert."
"Akzeptanzkriterien für Tetrahydrofuran sollten der Bewertung des Lipidstoffes ALC-0159 hinzugefügt werden, da es als Lösungsmittel in Schritt 2 der Synthese enthalten ist."
"Detaillierte Berichte über die Testvalidierung von Verunreinigungen und Lösungsmittelrückständen … sollten vorgelegt werden."
Diese Chemikalie wird hauptsächlich als Lösungsmittel für Kunststoffe und als Zwischenprodukt in organischen Synthesen verwendet. Sie gilt nach der Tabelle der Deutschen Gesetzlichen Unfallversicherung (DGUV) als krebserregend; in den USA bestätigt die Umweltbehörde EPA "suggestive Hinweise auf ein krebserregendes Potenzial".
Das Lipidmaterial der Nanoteilchen birgt noch weitere Risiken der Krebsgefahr. Im EMA-Bewertungsbericht steht auf S. 50, dass im Herstellungsprozess der Lipidkomponente ALC-0159 die als Krebserreger eingestuften Stoffe Acetamid, Dioxin sowie Polyethylenoxid als ungewolltes Nebenprodukt entstehen können (alle drei auf der Liste der DGUV). Laut EMA wird "erwartet", dass sie bei einer zweimaligen Dosis allerdings nur in unschädlichen Mengen vorkommen (Autorenanfrage an die EMA, Nr. ASK-98501 und ASK-98500). Eine dritte Booster-Dosis ab 18 Jahren erlaubte die EMA laut Presseerklärung vom 4. Oktober trotz "begrenzter Sicherheitsdaten" frühestens sechs Monate nach der zweiten Dosis.
Verunreinigung durch unvollständiges RNA-Material
Neue Studien belegen, dass biochemische Reaktionen des Genmaterials mit der Lipidhülle dessen Fragilität erhöhen und Teile davon in Bruchstücke zerfallen. Sie gelten als Verunreinigung. Zitate aus dem EMA-Bericht:
"Verkürzte (trunkierte) RNA-Spezies gelten als produktbezogene Verunreinigungen und sind … bei der Herstellung zu erwarten."
"Die hohen Konzentrationen dieser Verunreinigungen spiegeln die Instabilität der RNA wider, die zur Erzeugung von RNA-Fragmenten … führt."
"Diese Formen sind schlecht charakterisiert, und die begrenzten Daten zur Proteinexpression decken die Unsicherheiten in Bezug auf das Risiko der Translation von anderen Proteinen/Peptiden als dem beabsichtigten Spike-Protein nicht vollständig ab."
Das "Risiko der Translation" durch verkürzte Genpartikel bedeutet, sie könnten auf die genetische Gesamtinformation der RNA-Substanz in den Nanoteilchen Einfluss nehmen und unerwartete allergische oder sonstige Reaktionen hervorrufen oder aber die Gesamtwirkung des Genmaterials schwächen. Dagegen argumentieren die Hersteller, es sei "zwar nicht bestätigt, doch unwahrscheinlich", dass diese abweichenden RNA-Fragmente die genetische Botschaft verändern, da sie in ihrer Anzahl der intakten und immunstärkeren Potenz des RNA-Spike-Proteins unterlegen seien. Es habe sich außerdem gezeigt, dass keine Bioreaktionen dieser Art stattfinden, solange die Gefriertemperaturen korrekt eingehalten werden.
Die EMA bestätigte dem britischen Wissenschaftsportal BMJ,
"dass die Wirksamkeit des Impfstoffs vom Vorhandensein geeigneter Mengen intakter mRNA abhängt".
Nachforschungen des Portals ergaben, dass die FDA, die EMA, das kanadische Gesundheitsministerium und die britische Gesundheitsbehörde einen gemeinsamen Standard für den Prozentsatz der mRNA-Integrität vereinbart hatten. Sie waren jedoch nicht bereit, The BMJ mitzuteilen, welchen konkreten Prozentsatz sie für notwendig halten, um die Effektivität dieser Medikamente zu garantieren. Das sei vertraulich. Auch die Hersteller mehrerer Gen-Vakzine mauerten. Tenor: "Die Akzeptanzkriterien für die Spezifikationsgrenzen sind kommerziell vertraulich."
Die Antworten signalisieren Unsicherheit. Natürlich handelt es sich um ein streng wissenschaftliches Thema, das sowohl die Effektivität als auch unerwartete Immunreaktionen wie z. B. Anaphylaxie beinhaltet. Genau genommen hängt die Qualität der Gen-Impfstoffe an diesem seidenen Faden.
So sahen es auch die EMA-Experten, die an der Voraussetzung für die bedingte Zulassung von Comirnaty arbeiteten. Im Assessment-Report vom 19. Februar 2021 steht auf S. 29 trotz weitgehend zufriedenstellender Informationen:
"... die Akzeptanzkriterien wurden für die Potenz (des Spike-Proteins), für die RNA-Integrität, die RNA-Einkapselung, für den Lipidgehalt (der Nanopartikel) und die Polydispersität (der RNA-Bruchstücke) verschärft."
Und:
"Als Teil der Voraussetzungen, um die bedingte Zulassung zu erhalten, muss der Antragsteller zusätzliche Informationen bereitstellen, um die Verbesserung der Kontrollstrategie zu gewährleisten. Das ist Teil der 'Speziellen Verpflichtungen (SO)', die im zweiten Quartal 2021 zu erfüllen sind." (Siehe Tabelle aller SOs S. 36)
Die Anforderungen an die Kontrollpräzision werden trotz der zu diesem Zeitpunkt bereits vereinbarten 21 Prüftests so gestellt und zeigen die Unsicherheiten der Nano-RNA-Technik.
An dieser Stelle sei eine neue Studie vom 21. September 2021 genannt. Demnach sind solche Verunreinigungen mit herkömmlichen Techniken schwierig zu identifizieren. Zitat:
"Dies stellt eine Lücke in der Qualitätskontrolle von mRNA-Lipidnanopartikeln während der Herstellung dar, insbesondere was die Konsistenz und Aktivität des resultierenden Arzneimittelprodukts betrifft."
Die Studie mahnt vor einem Aktivitätsverlust des Genmaterials und damit der Wirksamkeit.
Diese Forschungsarbeit stellt die bisherigen spezifischen Prüfsysteme der Produktion stark infrage. Wie stehen die Wissenschaftler der EMA zu den neuen Erkenntnissen? Es sind keine Stellungnahmen bekannt, doch die Impferlaubnis wurde seitdem auf Kinder ab 12 Jahren ausgeweitet.
Vergleichbarkeit des Impfstoffs der Testreihen und des kommerziellen Impfstoffs
Zitate:
"Wirksamkeit, Sicherheit und Immunogenität wurden mit klinischen Chargen des Impfstoffs aus Verfahren 1 nachgewiesen. Die kommerziellen Chargen werden nach einem anderen Verfahren hergestellt (Verfahren 2)."
"Weitere Daten wurden angefordert, um Rückschlüsse auf die Konsistenz der Herstellung des Endprodukts zu ziehen."
"Die Vergleichbarkeit zwischen dem kommerziellen Endprodukt und dem klinischen Endprodukt ist für die geprüften Eigenschaften hinreichend nachgewiesen und unterliegt einer besonderen Verpflichtung [des Herstellungsprozesses]."
Die nicht eingehaltenen Verpflichtungen von Pfizer/BioNTech
In der aktualisierten Produktbeschreibung des Impfstoffes Comirnaty vom 14. Oktober 2021 im Anhang II, S. 39 sind die nicht erfüllten "Speziellen Verpflichtungen" der Hersteller angezeigt. Es handelt sich um fünf Themenbereiche, die allesamt eng an die Vergabe der bedingten Zulassung geknüpft sind. Pfizer/BioNTech muss demnach Zwischenberichte im März vorlegen und bis spätestens Juli die geforderten Problemlösungen im Herstellungsbereich umgesetzt haben. Doch mit Ausnahme der Anforderung SO3, die nun in der Liste nicht mehr vorhanden ist, haben die Firmen die restlichen vier nicht eingelöst (Autorenanfrage an die EMA, ASK 98498).
Welche juristischen Konsequenzen ergeben sich daraus? Müsste die bedingte Zulassung von Comirnaty nicht entsprechend ausgesetzt werden, solange die Voraussetzungen dafür nicht gegeben sind? Können Menschen gezwungen werden, sich mit einem solchen Medikament "therapieren" zu lassen? Nach der europäischen Gesetzesnorm sind diese Speziellen Verpflichtungen eine "rechtmäßige (legale) Anforderung" des Zulassungsverfahrens.
Verunreinigungen für schwere Impffolgen ursächlich?
Nach allen vorgefundenen Informationen – von denen nur ein Bruchteil in diesem Artikel behandelt werden kann – ist zu prüfen, ob die im ersten EMA-Evaluierungsbericht aufgezeigten verschiedenen Arten von Verunreinigungen mit den weltweit verzeichneten starken bis tödlichen Impfreaktionen zusammenhängen, ob sie für den hohen Prozentsatz an Impfdurchbrüchen und den raschen Rückgang der Effektivität mitverantwortlich sind und ob künftige Spätfolgen daraus resultieren können. Diese wissenschaftliche Studie hätte seit Beginn der Impfkampagne durchgeführt werden müssen.
Des Weiteren sollte geklärt werden, ob elektronenmikroskopische Untersuchungen auf Verunreinigungen des Impfstoffes am Endpunkt von Produktion und Verteilung sowie zum Zeitpunkt der Verabreichung in die Routinekontrollen der Chargen gehören.
GMP-Zertifikate für die Herstellungs- und Prüfstandorte
Im Verlauf des Arbeitsprozesses zur bedingten Zulassung wurden Verfahrensweisen zur Prüfkontrolle des Fertigproduktes definiert. Laut Bericht erhielten die zum damaligen Zeitpunkt registrierten Herstellungs- und Prüfstandorte das Zeugnis der "Guten Herstellungspraxis (GMP)".
Zitate:
"Zusammenfassend lässt sich sagen, dass für alle Produktionsstätten von Wirkstoffen und Fertigprodukten entsprechende Herstellungsgenehmigungen und GMP-Zertifikate vorhanden sind."
"Der Wirkstoff wird sowohl von Wyeth BioPharma Division, Andover, USA als auch von BioNTech Manufacturing GmbH, Mainz, Deutschland und Rentschler Biopharma SE, Laupheim, Deutschland sowie von Pfizer Manufacturing in Puurs, Belgien hergestellt und kontrolliert."
Die Anzahl der Firmen, die sowohl fertige Lipidnanopartikel als auch einzelne Zusatzstoffe liefern, hat sich bis heute vervielfacht.
Am 5. Februar erklärte die Firma Merck KGaA, dass sie verstärkt die benötigten Lipide für BioNTech übernehmen werde. BioNTech produziert in der früheren Anlage von Novartis in Marburg Nanolipide. Die Lipidproduktion der Firma Evonik Industries läuft an zwei Standorten in Deutschland für BioNTech. Das britische Chemieunternehmen Croda erhöhte seine Produktion in der Tochtergesellschaft Avanti Polar Lipids in Alabama, um Pfizer zu beliefern. Im Juni kam die Firma Allergopharma GmbH & Co. KG in Reinbek dazu, Novartis Pharma lässt in einem Werk in der Schweiz produzieren. Die Standorte werden in verschiedenen Phasen des Prozesses Herstellungsschritte für Fertigprodukte vornehmen.
Die Hersteller wählen ihre Chargen selbst aus, prüfen sie selbst und sollten ihre Daten an das Paul-Ehrlich-Institut (PEI) oder an andere europäische Prüfbehörden senden. Bis zum 31. August galt allerdings eine befristete EMA-Ausnahmeregelung: Die Prüftests der Chargen wurden ausgelagert – an einen Standort in den USA.
RT DE bemüht sich um ein breites Meinungsspektrum. Gastbeiträge und Meinungsartikel müssen nicht die Sichtweise der Redaktion widerspiegeln.
Mehr zum Thema - Pfizer-Wissenschaftler: "Ihre Antikörper sind wahrscheinlich besser als der Impfstoff"
Quellen:
Bewertungsstudie der EMA für die bedingte Zulassung von Comirnaty Dezember 2020
Produktbeschreibung Comirnaty 14.10.21
Liste der Dt.Unfallversicherung zu Krebserregern
Umweltagentur der USA, EPA: Liste krebserzeugender Stoffe
Neue Studie über schwierige Qualitätskontrollen für Nano-Lipide
EMA erlaubt am 4.Oktober 3. Dosis
Auch die Firma MERCK produziert Lipid-Nanopartikel
Normen des PEI nach dem Medikamentengesetz
The EMA covid-19 data leak, and what it tells us about mRNA instability
Durch die Sperrung von RT zielt die EU darauf ab, eine kritische, nicht prowestliche Informationsquelle zum Schweigen zu bringen. Und dies nicht nur hinsichtlich des Ukraine-Kriegs. Der Zugang zu unserer Website wurde erschwert, mehrere Soziale Medien haben unsere Accounts blockiert. Es liegt nun an uns allen, ob in Deutschland und der EU auch weiterhin ein Journalismus jenseits der Mainstream-Narrative betrieben werden kann. Wenn Euch unsere Artikel gefallen, teilt sie gern überall, wo Ihr aktiv seid. Das ist möglich, denn die EU hat weder unsere Arbeit noch das Lesen und Teilen unserer Artikel verboten. Anmerkung: Allerdings hat Österreich mit der Änderung des "Audiovisuellen Mediendienst-Gesetzes" am 13. April diesbezüglich eine Änderung eingeführt, die möglicherweise auch Privatpersonen betrifft. Deswegen bitten wir Euch bis zur Klärung des Sachverhalts, in Österreich unsere Beiträge vorerst nicht in den Sozialen Medien zu teilen.